Chemical Box : VSEPR
というわけで
少し化学が得意になり始めたぐらいの高校生にアンチの多い*1『ナントカの新研究』では、「SCIENCE BOX」というコラムがあってそこで高校の指導範囲を少し超えたような内容が扱われています。卒業とともに部活の後輩の誰かにあげてしまったので今はもう手元に無いため、どんなこと書いてあったのか全く覚えていません&確認が取れませんが。
そんな感じのノリで、主に化学グランプリとかその辺りのことを考えている高校生を想定読者に据えた化学系の記事を書いてみようかな、と思ってみた次第です。
今回はVSEPRについてです。中学校で化学部に入って初めて受けた授業で導入された概念で、以来自分が化学系の授業をする際には最初にデモ的に使ったりもしている、お気に入りの概念ですね。
目次
VSEPRとは
Valence Shell Electron Pair Repulsion model (原子価殻電子対反発理論)のことをここでは指します。分子の形を予測するのに使える理論になります。H2O分子の形が折れ線形だったり、CO2分子の形が直線形だったりするのも、この理論で説明出来ます。大学受験化学で時々聞かれる程度の分子の形状なら覚えていなくてもVSEPRから順当に導けるので、その点でも使えるかもしれないですね。
VSEPRで最も重要なのは、
原子の持つ電子対(に類するグループ)は、互いに出来るだけ離れようとする。
という考え方です。
その上、
- 非共有電子対は、共有電子対よりも反発力が大きい。
- 二重結合や三重結合等は、一つのグループとして考える。
という点も考慮して、分子の形を予測していきます。
互いに出来るだけ離れる…って?
これは、電子対(に類するグループ)の数でほぼほぼ確定するので、それを先に示しておきます。
2
直線形です。どう考えてもそうなので図は省略します。
3
正三角形状になります。

4
正四面体状になります。

5
これが少し注意が必要になりますが、一先ず図を出します。三方両錐形と呼ばれます。

これは、正三角形の中心に垂直に串を刺したような形状になっています。2~4本を互いに離れるように配置したときと違って、今回だと正三角形状の3本(エカトリアル)と、それに垂直な2本(アキシアル)が別の状態になっていますね。
自身以外の線との間の角度を見てみると、
エカトリアル : 120°×2 / 90°×2
アキシアル : 90°×3 / 180°×1
になっています。
6
正八面体状になります。

VSEPRを運用してみよう
以下の順序に従って、実際にVSEPRで分子の形を予測してみましょう。
- 形を考える分子の電子式(或いは、非共有電子対を含めた構造式)を書く。
- 着目する原子の電子対(に類するグループ)数を数える。
- 電子対(に類するグループ)が互いに空間的に最も離れるような配置を考える。
- 非共有電子対は、共有電子対(に類するグループ)よりも反発力が大きいことを考慮に入れて、原子を配置する。
CH4分子
構造式

電子対(に類するグループ)数
分子の形を予測するにはC原子に着目すれば良いですね。今回は「4」です。
空間配置
「4」ということで、正四面体状になりますね。
H2O分子
構造式

電子対(に類するグループ)数
分子の形を予測するにはO原子に着目すれば良いですね。今回は「4」です。
空間配置
「4」ということで、正四面体状になりますね。
非共有電子対の考慮
一先ず2つのHを正四面体の2つの頂点に配置することになります。

そして、非共有電子対の方が共有電子対よりも反発力が大きいので、H-O-Hの結合角が元々の約109.5°から狭められて…

この様になります。
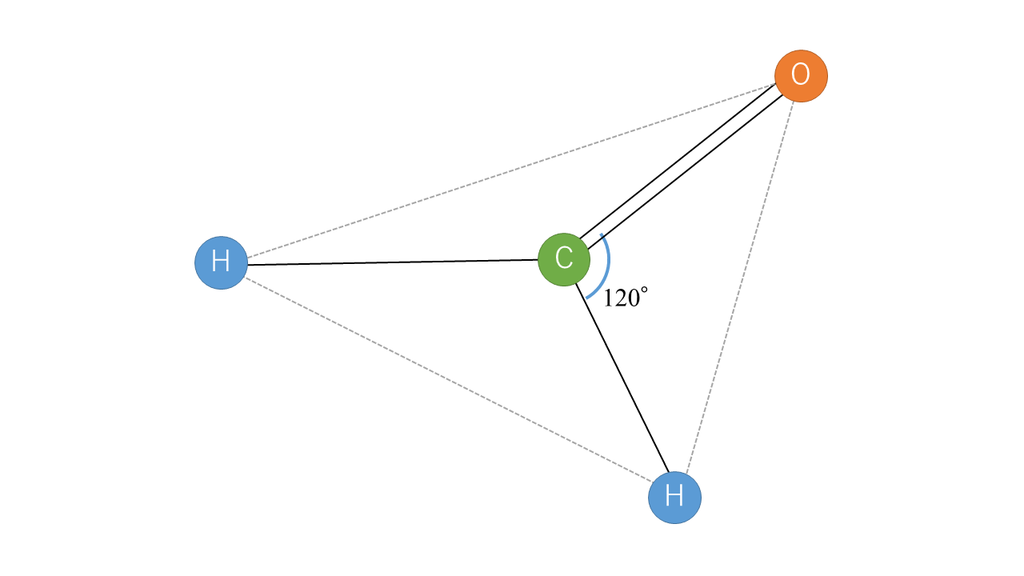
HCHO分子
構造式

電子対(に類するグループ)数
分子の形を予測するにはC原子に着目すれば良いですね。今回は「3」です。
空間配置
「3」ということで、正三角形になりますね。
PCl5分子
構造式

電子対(に類するグループ)数
分子の形を予測するにはP原子に着目すれば良いですね。今回は「5」です。
※高校までだと、ほぼ全ての分子について、分子中の原子の価電子数は8or2になっていますが、実際にはそれ以外の価電子数の原子を含んだ分子も存在します。その一例が、このPCl5です。
空間配置
「5」ということで、三方両錐形になりますね。
SF4分子
構造式

電子対(に類するグループ)数
分子の形を予測するにはS原子に着目すれば良いですね。今回は「5」です。
空間配置
「5」ということで、三方両錐形になりますね。
非共有電子対の考慮
非共有電子対×1と、共有電子対×4を三方両錐形に配置していきましょう。
さて、非共有電子対はどこに入るでしょうか?
アキシアルの位置とエカトリアルの位置にそれぞれ非共有電子対を配置した場合を考えると、エカトリアルの位置に非共有電子対を配置したほうが反発が小さくて済むので、エカトリアルの位置に非共有電子対を配置しましょう。
…と、「周りの電子対との干渉を考えるとエカトリアルの方がアキシアルより反発が小さい」というのが自明として扱われている教科書が多いです(少なくとも私はコレ以上に踏み入った解説を見たことがない)。でもこれ、それほど自明なことでしょうか? 私自身は「まぁ、そりゃそうか」程度で納得しはしましたが、VSEPRを誰かに教えている時にこの点をツッコまれてもおかしくないよなぁという認識です。
以下は、それを頑張って説明(?)しようと試みている部分です。怪しいので、無視していただいて構いません。
とても荒い近似として、電子対を全て一つの点電荷とみなした上でポテンシャルエネルギーを考えてみることにしましょう。また、中心原子と各電子対との距離は等しいとしましょう。
この条件で、他の電子対の影響でアキシアル/エカトリアルの位置に有る電子対が持つ位置エネルギー(それぞれ、
としましょう)を考えてみます。
各電子対を点電荷に近似した時のそれぞれの電荷は等しいので、位置エネルギー
と距離
の関係は
と見てしまえます。
すると、
となるので、、即ちアキシアルの位置にある電子対のほうが、エカトリアルの位置にある電子対よりも不安定になることが分かります。
さて、話を戻しましょう。エカトリアルの位置に非共有電子対を配置するということで、一先ず以下のようにSF4分子の形を推測できます。

最後に非共有電子対の反発力の強さを考慮すると、SF4分子の形は以下のようだと推測できます。

練習問題
以下の分子、イオンの形を予測してみましょう。
- NH3分子
- CO2分子
- BH3分子
- SF6分子
- I3
イオン
ちょっとした補足
VSEPRはあくまでも「簡単に」分子の形を予測する程度のもので、例えばH2O分子の正確な結合角がVSEPRだけからわかるわけではないです。
また、PCl5分子やSF4分子等の三方両錐形分子に関してはベリー擬回転を起こすせいで、NMRの時間分解能ではアキシアル/エカトリアルの位置にある原子を区別できない等の話もあります。
最後に
VSEPRは、高校化学等で構造式や電子式に触れ始めた人がその知識を応用して、よりリアルに分子の形を捉えられる面白い理論だと思います。
こんな感じで、Chemical Boxの記事を定期的に出していけたらな、と。
記事の内容に関して何か、或いはリクエスト等ありましたら、コメントなり私のTwitterアカウント[@sGya_youtoo]までご連絡なり頂ければ幸いです。
参考
アトキンス物理化学要論 第5版
シュライバーアトキンス無機化学(上) 第4版